|
| |
|
| |
H |
|
| |
|
|
| |
Wasserstoffisotopenverhältnis, Wasserstoff hat zwei stabile Isotope (1H = Protonium, H; 2H= Deuterium, oft als D abgekürzt) mit den durchschnittlichen Häufigkeiten 99,9844% und 0,0156%, die aber durch Isotopenfraktionierungsprozesse verändert werden. Durch Höhenstrahlung wird in der Atmosphäre auch das radioaktive Wasserstoffisotop Tritium 3H (T) erzeugt. Dessen Gesamtmenge ist aber sehr klein und es zerfällt mit einer Halbwertszeit von 12,43 Jahren.
Wasserstoff ist primär nur in geringen Mengen in Mineralen und Gesteinen enthalten, daher wirken sich Austausch- und Kontaminationsprozesse mit Poren- und Formationswässern sehr stark auf das 2H/1H-Isotopenverhältnis aus. Fraktionierungsprozesse beim Wasserstoff sind aufgrund des grossen Massenunterschiedes (100%) ausserordentlich wirkungsvoll. Variationen des 2H/1H-Isotopenverhältnisses werden als δD-Wert in ‰ angegeben, bezogen auf den Standard SMOW. Die grosse Bandbreite der Wasserstofffraktionierung wird am δD-Wert von -428 ‰ für den Isotopenstandard SLAP (Standard Light Antarctic Precipitation) deutlich. Die extreme Zusammensetzung ist auf das verstärkende Zusammenwirken von Breiteneffekt (atmosphärische Zirkulation) und Höheneffekt (Gasfraktionierung durch Aufsteigen der Luftmassen bei gleichzeitig niedrigen Temperaturen) zurückzuführen. Als Reservoirs und Austauschpartner für den geochemischen Wasserstoffkreislauf stehen Atmosphäre, Hydrosphäre, Erdkruste (Granite, Metamorphite und Sedimente) und Teile des Erdmantels (Mid Ocean Ridge Basalt) zur Verfügung (Abb. 1).
Der geochemische Kreislauf des Wasserstoffs ist stark an den Wasserkreislauf und an biogene Prozesse im exogenen Bereich gebunden. Austauschreaktionen (und damit Fraktionierungsprozesse) zwischen magmatischen oder metamorphen Formationswässern mit Oberflächenwasser sind aber von grosser Bedeutung für die Herkunftsbestimmung letzterer. Andererseits können z.B. Kontaminations- oder Auslaugungsprozesse von Ozeanbodenvulkaniten durch Meerwasser oder sonstigen hydrothermalen Systemen mit meteorischen Wässern Auskunft über deren Genesebedingungen geben. Ein Beispiel unter Einbeziehung der Sauerstoff-Isotopenverhältnisse gibt Abb. 2 (Sauerstoffkreislauf, 16O/18O). D/H-Werte eignen sich auch für die Beschreibung der Temperaturbedingungen bei Verwitterungsund Diageneseprozessen von Mineralen. Bei kalten Bedingungen durch chemische Verwitterung entstandene Tonminerale haben niedrigere Wasserstoff- und Sauerstoffisotopenverhältnisse als solche, die bei höheren Temperaturen entstanden sind (Abb. 3). Taylor (1974) beschreibt 6 Typen von natürlichen Wässern (terrestrische Wässer, Abb. 3):
a) meteorische Wässer: Sie haben die grösste δD-Bandbreite, die über folgende Beziehung mit der
Sauerstoffisotopie verknüpft ist: δD‰ = 8,17·δ18O‰+10,35.
Diese Beziehung wird auch als Niederschlagsgerade bezeichnet. b) Meerwasser, SMOW; c)
geothermales Wasser: im Prinzip meteorisches Wasser, dass aber durch Austauschprozesse mit
durchflossenem Gestein höhere δ18O-Werte hat; d) Formationswasser (mit grosser Bandbreite): eine Zweikomponentenmischung aus breitenabhängiger Isotopie von meteorischem Wasser und
gesteinsabhängiger Isotopie der Porenfluids; e) magmatisches Wasser; f) metamorphes Wasser.
Die Beweisführung, dass Wasser für die Veränderung/Kontamination magmatischer und metamorpher Wässer verantwortlich ist, erfordert die kombinierte Untersuchen der Sauerstoff- und
Wasserstoffisotope. Die markanteste biogene Fraktionierung von Wasserstoff, aber auch von O, N, C
und S passiert oft schon bei der ersten (primären) Produktion von Biomasse. Eine weitere, aber nicht
mehr so ausgeprägte Fraktionierung tritt dann in der Nahrungskette auf. Grundsätzlich wird das
leichtere Isotop bevorzugt(kinetischer Effekt). In marinen Algen ist eine Fraktionierung um -100 bis
-150‰ charakteristisch, terrestrische Pflanzen zeigen Werte zwischen -86 und -120‰. Das
Wasser-Vorratsvolumen für die pflanzliche Wasserstoff-Fraktionierung stellt eine Mischung aus den
Reservoirs Grundwasser (als Mischung aus Sommer- und Winterniederschlägen plus
Gesteins-Formationswasserkontamination) und Sommerniederschlägen (nur in dieser Zeit ist die
Pflanze signifikant aktiv) dar (Abb. 4). Im Wurzel- und Leitbündelbereich ("vor der Photosynthese")
spiegelt die Wasserstoffisotopie noch die Mischung der Reservoirs wider, in der Blattflüssigkeit und
dem Pflanzengewebe zeigt sich dann die biogene Fraktionierung des Wassers in "schweres
Residuum" (+30‰) und "leichte Biomasse" ( < -60‰) als durch die Pflanze verwertetes, leichtes
Wasser. Dass Pflanzen aus kühleren Klimaten stärker an Deuterium verarmt sind (δD negativer) als
solche aus warmen oder gemässigten Klimazonen, ist auf einen Reservoir-Effekt zurückzuführen. Auch in der organischen Geochemie findet die Wasserstoffisotopie Anwendung. Oft in Kombination
mit anderen Isotopensystemen können genetische und herkunftsspezifische Parameter bestimmt
werden. Im allgemeinen sind lipidreiche Kerogene, Öle und Kohlen stärker an Deuterium verarmt als
"normale", deren δD dem der ursprünglichen Biomasse noch sehr ähnlich ist (Abb. 5). WL
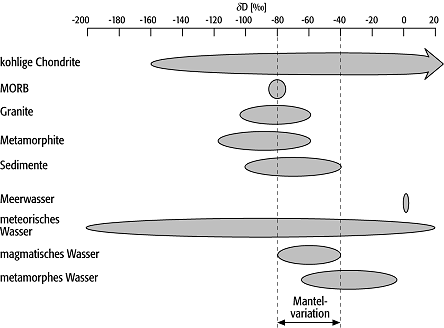 2H/1H 1: natürliche Wasserstoff-Isotopenreservoirs. Die Bandbreite der Reservoirs "meteorisches Wasser" und "kohlige Chondrite" spiegelt die extreme Fraktionierung aufgrund der grossen Massenunterschiede wider. 2H/1H 1: natürliche Wasserstoff-Isotopenreservoirs. Die Bandbreite der Reservoirs "meteorisches Wasser" und "kohlige Chondrite" spiegelt die extreme Fraktionierung aufgrund der grossen Massenunterschiede wider.
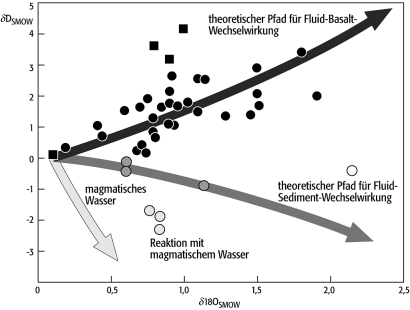 2H/1H 2: Sauerstoff- und Wasserstoff-Isotopenverhältnisse bei hydrothermalen Ozeanbodenprozessen: theoretische Pfade für Fluid-Sediment- und Fluid-Ozeanbodenbasalt-Wechselwirkung und analysierte Proben. Hell gekennzeichnete Analysen zeigen zusätzlich eine Reaktion mit magmatischem ("juvenilem") Wasser. 2H/1H 2: Sauerstoff- und Wasserstoff-Isotopenverhältnisse bei hydrothermalen Ozeanbodenprozessen: theoretische Pfade für Fluid-Sediment- und Fluid-Ozeanbodenbasalt-Wechselwirkung und analysierte Proben. Hell gekennzeichnete Analysen zeigen zusätzlich eine Reaktion mit magmatischem ("juvenilem") Wasser.
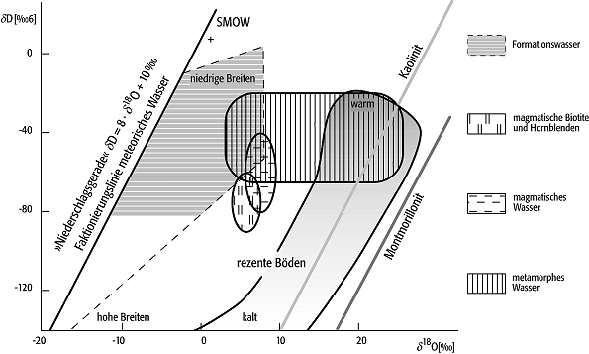 2H/1H 3: δD-δ18O-Variationsdiagramm mit Diskriminationsfeldern für Formationswässer und Fluids sowie temperaturabhängiger Verwitterung. 2H/1H 3: δD-δ18O-Variationsdiagramm mit Diskriminationsfeldern für Formationswässer und Fluids sowie temperaturabhängiger Verwitterung.
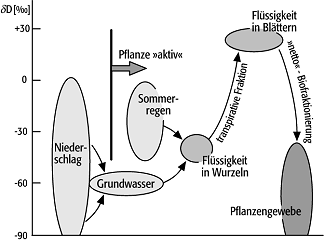 2H/1H 4: Das Wasser-Vorratsvolumen für die pflanzliche Wasserstoff-Fraktionierung stellt eine Mischung aus den Reservoirs Grundwasser, Sommer- und Winterniederschläge plus Gesteins-Formationswasserkontamination dar. 2H/1H 4: Das Wasser-Vorratsvolumen für die pflanzliche Wasserstoff-Fraktionierung stellt eine Mischung aus den Reservoirs Grundwasser, Sommer- und Winterniederschläge plus Gesteins-Formationswasserkontamination dar.
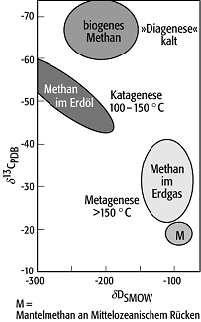 2H/1H 5: δD-δ13C-Variationsdiagramm zur Unterscheidung von Methanquellen. Biogenes Methan ist bei der Diagenese entstanden, Erdöl begleitendes Methan im "Erdölfenster/Katagenese" und Methan im Erdgas ist durch eine abnehmende Fraktionierung zwischen Methangas und residualen Kerogenen bei der Metagenese (T > 150°C) gekennzeichnet (PDB = Peedee Belemnit Standard, SMOW = Standard Mean Ocean Water). 2H/1H 5: δD-δ13C-Variationsdiagramm zur Unterscheidung von Methanquellen. Biogenes Methan ist bei der Diagenese entstanden, Erdöl begleitendes Methan im "Erdölfenster/Katagenese" und Methan im Erdgas ist durch eine abnehmende Fraktionierung zwischen Methangas und residualen Kerogenen bei der Metagenese (T > 150°C) gekennzeichnet (PDB = Peedee Belemnit Standard, SMOW = Standard Mean Ocean Water). |
|
| |
|
|
| |
Ein Bookmark auf diese Seite setzen:
|
|
| |
|
|
| |
<< vorheriger Begriff |
|
nächster Begriff >> |
|
|
|
|
|
| |
|
|
|
|