| |
1) Allgemein: durch Ausgasung aus der festen, gelösten oder flüssigen Stoffphase überführte Chemikalien. Die Ausbreitung von Chemikalien im Untergrund wird von folgenden komplexen physikochemischen Eigenschaften gesteuert: a) Fliesseigenschaften flüssiger Schadstoffphasen, b) Löslichkeitsverhalten der Schadstoffe und c) Flüchtigkeit der Chemikalien (Reinphase oder aus der wässrigen Lösung). Die Flüchtigkeit ist dabei eine komplexe Eigenschaft und beschreibt die Möglichkeit eines Stoffes, in die Dampfphase überzugehen. Dabei sind zwei Prozesse zu unterscheiden, die von verschiedenen physikochemischen Parametern gesteuert werden: a) Stoffübergang von der gelösten, adsorbierten oder reinen Schadstoffphase in die Dampfphase, b) Ausbreitung in der Gas- bzw. Dampfphase. Der Stoffübergang von der reinen Schadstoffphase in die Dampfphase wird meist über den Dampfdruck der Substanz abgeschätzt. Die Flüchtigkeit eines Stoffes wird jedoch im wesentlichen neben seinem Dampfdruck durch die Dampfdichte und die Henry-Konstante KH bestimmt. Der Dampfdruck hängt von der mittleren kinetischen Energie und der Konzentration der Dampfteilchen ab, die beide nur über die Temperatur gesteuert werden. Er nimmt bei den meisten organischen Chemikalien mittleren Molekulargewichtes um das 3 bis 4fache zu, wenn die Temperatur um 10°C steigt. Eine Temperaturerhöhung hat eine erhöhte Verdampfungsgeschwindigkeit zur Folge, wodurch es zu einer Konzentrationserhöhung der Dampfmoleküle kommt. Dies und die erhöhte kinetische Energie der Dampfmoleküle bei Temperaturerhöhung führen zu einer Zunahme des Dampfdruckes. So beträgt z.B. der Dampfdruck von Wasser bei 20°C 2330 Pa, bei 100°C 101.300 Pa. Flüssigkeiten mit schwachen intermolekularen Anziehungskräften besitzen relativ hohe Dampfdrücke. Das Lösungsmittel Diethylether weist beispielsweise bei 20°C einen Dampfdruck von 58.900 Pa auf. Generell gilt, je höher der Dampfdruck einer Flüssigkeit ist, desto höher ist seine Flüchtigkeit. Substanzen mit einem Dampfdruck von mehr als 70 Pa sind als gut flüchtig einzustufen.
In der Regel liegen im Boden Schadstoffgemische mit Komponenten unterschiedlicher Löslichkeit und Flüchtigkeit vor. Der Dampfdruck einer Komponente über dem Schadstoffgemisch ist eine Funktion ihres Anteiles am Gemisch (Molenbruch) und ihres Dampfdruckes in Reinphase. Bei guter Durchmischung ist keine nennenswerte Verringerung bzw. Erhöhung der Verdunstungsraten im Vergleich zur Verdunstung der reinen Substanz zu erwarten. Theoretisch ist allerdings eine Einkapselung der leichtflüchtigen Komponente möglich, wenn an der Phasengrenze ein im Schadstoffgemisch gelöster Feststoff geringer Flüchtigkeit durch Überschreiten der Sättigungskonzentration infolge verstärkter Ausdampfung der leichtflüchtigen Lösung ausfällt. Dieser Effekt dürfte für Schadstoffphasen im Porenraum des Bodens nur eine untergeordnete Rolle spielen, könnte aber bei Schadstoffanreicherungen in grösseren Hohlräumen (z.B. Rinnen, Klüfte) des Untergrundes von Bedeutung werden. Generell gilt, dass eine Substanz mit hohem Dampfdruck und hoher Wasserlöslichkeit weniger zur Ausdampfung neigt als eine Chemikalie mit hohem Dampfdruck, aber geringer Wasserlöslichkeit. Der Einfluss der Wasserlöslichkeit auf die Verdampfungsneigung kann über die Henry-Konstante erfasst werden, in der die Flüchtigkeit als Funktion von Wasserlöslichkeit und Dampfdruck beschrieben wird. Substanzen mit hoher Wasserlöslichkeit und hohem Dampfdruck haben eine geringere Flüchtigkeit als Substanzen mit geringer Wasserlöslichkeit und hohem Dampfdruck. Der Zusammenhang zwischen Wasserlöslichkeit und Dampfdruck auf die Flüchtigkeit über die Henry-Konstante wird folgendermassen beschrieben:
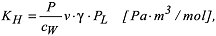 wobei KH = Henry-Konstante (beschreibt das Verhältnis zwischen Partialdruck in der Luft und der Gleichgewichtskonzentration im Wasser), P = Partialdruck der Substanz in der Gasphase , cW = wobei KH = Henry-Konstante (beschreibt das Verhältnis zwischen Partialdruck in der Luft und der Gleichgewichtskonzentration im Wasser), P = Partialdruck der Substanz in der Gasphase , cW =
Konzentration der Substanz im Wasser = Wasserlöslichkeit [mol/m3], v =molares Volumen der Lösung
[mol/m3], γ =Aktivitätskoeffizient in der flüssigen Phase und PL = Dampfdruck der Reinsubstanz
ist.
Da in der Praxis normalerweise Schadstoffkonzentrationen anstelle von Partialdrücken gemessen werden, wird die dimensionslose Form der Henry-Konstante bevorzugt angegeben: wobei KH = Henry-Konstante (beschreibt das Verhältnis der Gleichgewichtskonzentration der Substanz in Luft zu der im Wasser), cA =Konzentration der Substanz in der Luft [mol/m3], cW = Konzentration der Substanz im Wasser [mol/m3], R =Gaskonstante=8,314 Pa·m3/(mol·K), T =
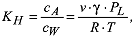 Temperatur [K]. Die stoffspezifische Henry-Konstante ist relativ konzentrationsunabhängig, wird aber von der Temperatur, dem Druck und der Ionenstärke beeinflusst. Bei fallender Temperatur, steigendem Druck und hohen Gehalten an potentiellen Absorbenten sinkt KH, d.h. das Gleichgewicht verschiebt sich in Richtung des Wassers. Von Substanzen mit Henry-Konstanten grösser 1 Pa·m3/mol kann eine signifikante Verflüchtigung erwartet werden. Nach der Henry-Konstanten können Stoffe in folgende Flüchtigkeitsstufen eingeteilt werden: a) gering flüchtig: KH < 0,003 Pa·m3/mol, b) mittel flüchtig: KH = 0,003-100 Pa·m3/mol, c) stark flüchtig: KH > 100 Pa·m3/mol. Die wichtigsten flüchtigen Schadstoffe sind: LCKW, LHKW, VOC, VOX, FCKW, BTEX, Methan u.a. Der Eintrag von Gasen in den Boden wird massgeblich von der relativen Dampfdichte gesteuert. Die relative Dampfdichte ist eine dimensionslose Vergleichszahl bezogen auf die Dichte von Luft. Sie ist proportional der molaren Masse. Diese bezeichnet die Masse eines chemischen Elementes oder einer Verbindung, die 1 mol (6·1023) Atome bzw. Moleküle enthält und wird in g/mol angegeben. Die molare Masse dividiert durch 29 ergibt die relative Dampfdichte. Gase, die schwerer als Luft sind, können selbst bei absoluter Windstille mit der Bodenoberfläche in Kontakt kommen und entsprechend der Schwerkraft in den Porenraum des Bodens eindringen. Dagegen können Gase, die leichter als Luft sind, nur über Diffusion und eine rasche Adsorption an der Bodenoberfläche in den Untergrund eingetragen werden. Für die Ausbreitung in der Bodenluft spielt die Dampfdichte infolge der raschen Diffusion in der Gasphase nur eine untergeordnete Rolle. Als Mass für die Beweglichkeit der Gase können die Diffusionskoeffizienten herangezogen werden. Diese erreichen bei Gasen Werte in der Grössenordnung 10-4 bis 10-5 m2/s. Bei Flüssigkeiten sind die Diffusionskoeffizienten mit Werten um 10-9 m2/s um drei Zehnerpotenzen niedriger. Die Diffusionsgeschwindigkeit der Gasmoleküle ist um so höher, je kleiner die molaren Massen und je höher die Temperaturen sind. Nach dem Grahamschen Gesetz sind die Geschwindigkeiten (v1,2,...), mit denen Gase durch eine poröse Wand diffundieren, den Quadratwurzeln aus ihren molaren Massen umgekehrt proportional. Temperatur [K]. Die stoffspezifische Henry-Konstante ist relativ konzentrationsunabhängig, wird aber von der Temperatur, dem Druck und der Ionenstärke beeinflusst. Bei fallender Temperatur, steigendem Druck und hohen Gehalten an potentiellen Absorbenten sinkt KH, d.h. das Gleichgewicht verschiebt sich in Richtung des Wassers. Von Substanzen mit Henry-Konstanten grösser 1 Pa·m3/mol kann eine signifikante Verflüchtigung erwartet werden. Nach der Henry-Konstanten können Stoffe in folgende Flüchtigkeitsstufen eingeteilt werden: a) gering flüchtig: KH < 0,003 Pa·m3/mol, b) mittel flüchtig: KH = 0,003-100 Pa·m3/mol, c) stark flüchtig: KH > 100 Pa·m3/mol. Die wichtigsten flüchtigen Schadstoffe sind: LCKW, LHKW, VOC, VOX, FCKW, BTEX, Methan u.a. Der Eintrag von Gasen in den Boden wird massgeblich von der relativen Dampfdichte gesteuert. Die relative Dampfdichte ist eine dimensionslose Vergleichszahl bezogen auf die Dichte von Luft. Sie ist proportional der molaren Masse. Diese bezeichnet die Masse eines chemischen Elementes oder einer Verbindung, die 1 mol (6·1023) Atome bzw. Moleküle enthält und wird in g/mol angegeben. Die molare Masse dividiert durch 29 ergibt die relative Dampfdichte. Gase, die schwerer als Luft sind, können selbst bei absoluter Windstille mit der Bodenoberfläche in Kontakt kommen und entsprechend der Schwerkraft in den Porenraum des Bodens eindringen. Dagegen können Gase, die leichter als Luft sind, nur über Diffusion und eine rasche Adsorption an der Bodenoberfläche in den Untergrund eingetragen werden. Für die Ausbreitung in der Bodenluft spielt die Dampfdichte infolge der raschen Diffusion in der Gasphase nur eine untergeordnete Rolle. Als Mass für die Beweglichkeit der Gase können die Diffusionskoeffizienten herangezogen werden. Diese erreichen bei Gasen Werte in der Grössenordnung 10-4 bis 10-5 m2/s. Bei Flüssigkeiten sind die Diffusionskoeffizienten mit Werten um 10-9 m2/s um drei Zehnerpotenzen niedriger. Die Diffusionsgeschwindigkeit der Gasmoleküle ist um so höher, je kleiner die molaren Massen und je höher die Temperaturen sind. Nach dem Grahamschen Gesetz sind die Geschwindigkeiten (v1,2,...), mit denen Gase durch eine poröse Wand diffundieren, den Quadratwurzeln aus ihren molaren Massen umgekehrt proportional.
In erster Näherung können somit über die molaren Massen (m) der Verbindungen ihre relativen Geschwindigkeiten (v) abgeschätzt werden:
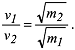 Die diffusive Ausbreitung im Untergrund wird massgeblich von pedogenen Parametern gesteuert. Im Vergleich zu diesen haben die substanzspezifischen Grössen einen vergleichsweisen geringen Einfluss auf die Diffusionskoeffizienten im Boden. 2) Lagerstättenkunde: beim Erhitzen einer Kohle unter Luftabschluss gas- und dampfförmig entweichende Zersetzungsprodukte der organischen Kohlensubstanz. Sie sind ein wichtiger Qualitätsparameter bei Steinkohlen. Wenn der Begriff als Inkohlungsparameter verwendet wird, erfolgt die Angabe bezogen auf wasser- und aschefreie Substanz [%(waf)]. Die diffusive Ausbreitung im Untergrund wird massgeblich von pedogenen Parametern gesteuert. Im Vergleich zu diesen haben die substanzspezifischen Grössen einen vergleichsweisen geringen Einfluss auf die Diffusionskoeffizienten im Boden. 2) Lagerstättenkunde: beim Erhitzen einer Kohle unter Luftabschluss gas- und dampfförmig entweichende Zersetzungsprodukte der organischen Kohlensubstanz. Sie sind ein wichtiger Qualitätsparameter bei Steinkohlen. Wenn der Begriff als Inkohlungsparameter verwendet wird, erfolgt die Angabe bezogen auf wasser- und aschefreie Substanz [%(waf)]. |
|