| |
das Löslichkeitsprodukt für Calcit beträgt 10-8,480 in reinem Wasser bei 298,15 K. Die Löslichkeit steigt mit sinkender Temperatur, steigendem Druck und steigendem Kohlendioxid-Partialdruck (Abb.). Insbesondere letzterer ist die entscheidende Grösse im Carbonat-Kohlendioxidsystem. Da CO2 bei der Calcitlösung aufgezehrt wird, ist diese unter CO2-limitierten Bedingungen (geschlossenes System) deutlich geringer als unter konstantem CO2-Partialdruck (offenes System).
Die Zunahme der Calcitlöslichkeit mit steigendem Druck und sinkender Temperatur bedingt, dass in Ozeanen unterhalb einer kritischen Wassertiefe Calcite vollständig aufgelöst werden. Sedimente, die unterhalb dieser Carbonat-Kompensations-Tiefe abgelagert werden, sind daher weitgehend carbonatfrei. Die Kinetik der Calcitlösung wird in Abhängigkeit von der Wasserstoffionenkonzentration von verschiedenen Mechanismen geprägt:
CaCO3+H+→Ca2++HCO3-(1) CaCO3+H2CO3-→Ca2++2HCO3-(2) CaCO3+H2O→Ca2++HCO3-+OH-(3) Reaktion (1) ist der transportbestimmte Protonenangriff in stark saurem Milieu, Reaktion (2) beschreibt die Abhängigkeit der Calcit-Löslichkeit vom pH und v.a. vom CO2-Partialdruck, und Reaktion (3) ist die Hydrolyse von Calcit bei hohen pH-Werten. Generell ist die Kinetik der Calcitlösung schnell genug, um unter thermodynamischem Gleichgewicht zu erfolgen. Hingegen ist die Calcitfällung deutlich verzögert und der Sättigungsindex vieler Grundwässer beträgt 0-0,3. Diese Übersättigung wird durch die Wirkung von Inhibitoren verursacht. Einer der wichtigsten ist Mg2+, dessen Adsorption an die Kristallitoberfläche das weitere Wachstum geordneter Calcitkristalle behindert. Erst bei sehr hoher Übersättigung kann Mg2+ in die Calcitstruktur eingebaut werden und es entstehen Mg-Calcite, die bis zu 30 Gew.-% Mg enthalten können. Die Aragonitfällung wird hingegen nicht durch Mg2+ behindert und begründet u.a. die geringere Übersättigung von Meerwasser mit seinem hohen Mg/Ca-Verhältnis hinsichtlich des Aragonits im Vergleich zu Calcit. Als Inhibitoren der Calcitfällung wirken auch Phosphat (ab ca. 1 μmol/l) und organische Säuren (ab ca. 10 μmol/l).
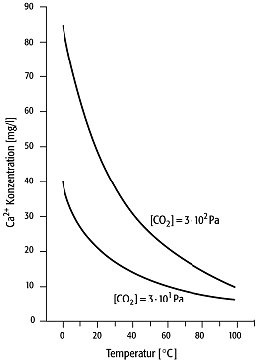 Calcit-Löslichkeit in Wasser: Abnahme der Calcitlöslichkeit mit steigender Temperatur und sinkendem CO2-Partialdruck. Die Ordinate zeigt die Ca2+-Konzentration der gesättigten Lösung im Gleichgewicht mit Calcitkristallen. Calcit-Löslichkeit in Wasser: Abnahme der Calcitlöslichkeit mit steigender Temperatur und sinkendem CO2-Partialdruck. Die Ordinate zeigt die Ca2+-Konzentration der gesättigten Lösung im Gleichgewicht mit Calcitkristallen. |
|