| |
acid mine drainage, AMD, acid rock drainage, ARD, bezeichnet Wässer mit einem sehr niedrigen pH-Wert unter ca. 3,5. Kennzeichnend ist ein hohes Redoxpotential (ca. >0,5 V) und eine hohe Lösungsfracht, die v.a. von hohen Sulfatkonzentrationen (bis über 20 g/l) geprägt ist. Saure Wässer entstehen durch die Oxidation von Sulfiden, deren Oxidationsprodukte Wasserstoffprotonen,
Sulfat und Metallkationen sind. Die an Pyrit (FeS2) studierten Prozesse weisen als Oxidationsmechanismus auf eine Adsorption von Sauerstoff an die Sulfidoberfläche und die anschliessende, entscheidend bakteriell katalysierte Oxidation von Fe(II) zu Fe(III), das nun wiederum sulfidischen Schwefel in mehreren Teilreaktionen zu Sulfat-Schwefel oxidiert und dabei wieder zu Fe(II) reduziert wird. Ratenlimitierend sind dabei die Bioaktivität und die Sauerstoffverfügbarkeit. Schematisch gilt:
FeS2+14Fe3++8H2O→15Fe2++2SO42-+16H+,
Fe2++H++1/4O2→Fe3++1/2H2O.
Das hohe Redoxpotential erlaubt oft eine Bildung von Fe(III)-Sekundärmineralen, sobald die pH-Werte auf 2,5-3 angehoben werden. Durch Adsortption an Sekundärminerale werden andere Ionenkonzentrationen ebenfalls vermindert. Wichtige Vertreter der Sekundärminerale sind neben den Fe(II)-Sulfaten die Fe(III)-Minerale Jarosit, Schwertmannit, Ferrihydrit und Goethit (Abb.). Die Bildung saurer Wässer ist eine gravierende Umweltauswirkung (besonders durch die Bergbauindustrie auf marin abgelagerten Kohlen und Metall-Sulfid-Lagerstätten), deren Vermeidung bzw. Behebung zunehmende Kosten verursacht. Eisenhydroxide.
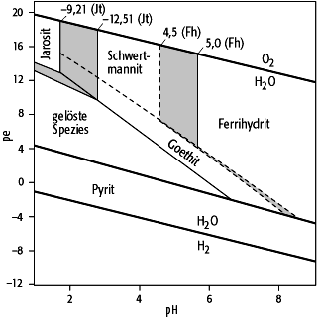 saure Wässer: Stabilitätsdiagramm verschiedener Fe(III)-Minerale (System Fe-S-K-O-H), die sich durch zunehmende Neutralisierung saurer Wässer bilden können. Metastabile Grenzen sind gestrichelt gezeigt. Für Jarosite und Ferrihydrit sind Feldgrenzen für verschiedene Löslichkeitsprodukte (angegeben als pK) dargestellt. saure Wässer: Stabilitätsdiagramm verschiedener Fe(III)-Minerale (System Fe-S-K-O-H), die sich durch zunehmende Neutralisierung saurer Wässer bilden können. Metastabile Grenzen sind gestrichelt gezeigt. Für Jarosite und Ferrihydrit sind Feldgrenzen für verschiedene Löslichkeitsprodukte (angegeben als pK) dargestellt. |
|