| |
chemische Systeme, in denen Reduktions- und Oxidationsvorgänge parallel ablaufen: Einer der Reaktionspartner stellt Elektronen zur Verfügung (wird oxidiert) und der andere nimmt diese Elektronen auf (wird reduziert). Das Redoxpotential lässt sich durch die Nernstsche Gleichung berechnen:
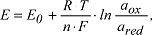 wobei E0 das Standardpotential, R die ideale Gaskonstante, T die Temperatur in Kelvin, n die Anzahl der übertragenen Elektronen, F die Faradaykonstante und aox bzw. ared die Aktivitäten der oxidierden und reduzierenden Substanzen sind. Bei Redoxreaktionen in Böden sind stets mehrere Partner beteiligt. Auch Wasser und seine Komponenten (Protonen und Hydroxidionen) sind an diesen Reaktionen beteiligt, daher sind Redoxreaktionen in starkem Mass pH-Wert abhängig. wobei E0 das Standardpotential, R die ideale Gaskonstante, T die Temperatur in Kelvin, n die Anzahl der übertragenen Elektronen, F die Faradaykonstante und aox bzw. ared die Aktivitäten der oxidierden und reduzierenden Substanzen sind. Bei Redoxreaktionen in Böden sind stets mehrere Partner beteiligt. Auch Wasser und seine Komponenten (Protonen und Hydroxidionen) sind an diesen Reaktionen beteiligt, daher sind Redoxreaktionen in starkem Mass pH-Wert abhängig. |
|