| |
nach L. Pauling auch als Resonanz bezeichnete Lehre zur Beschreibung der Bindungsverhältnisse in Molekülen, für die eine Zuordnung von einsamen und bindenden Valenzelektronenpaaren durch eine Valenzstrichformel nicht in befriedigender Weise möglich ist. Der Grundzustand dieser Moleküle wird durch Überlagerung der angebbaren Valenzstrichformeln (mesomere Grenzstrukturen, Valenzstrukturen) beschrieben. Die Grenzstrukturen stellen keine real existierenden Zustände des Moleküls dar, sondern dienen lediglich als Hilfsmittel, um die wirkliche Elektronenstruktur zu veranschaulichen. Die Überlagerung der Grenzstrukturen wird durch den Mesomeriepfeil (↔) zum Ausdruck gebracht. Die Mesomerie dient besonders zur Erklärung der Bindungsverhältnisse von Molekülen mit konjugierten Doppelbindungen, speziell aromatischer Verbindungen, z.B. des Benzols (Abb.). Von den jedem Kohlenstoff des Benzols zur Verfügung stehenden vier Elektronen bilden drei Elektronen Einfachbindungen zu den beiden benachbarten Kohlenstoffatomen und dem Wasserstoffatom. Das jeweils verbleibende Elektron der sechs Kohlenstoffe gehört einer ringübergreifenden Bindung an, welche als π-Bindung bezeichnet wird. Aufgrund der durch Mesomerie gebildeten π-Elektronen-Bindung erhält das aromatische Molekül eine besondere Stabilität.
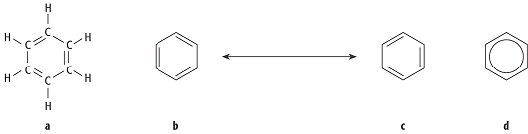 Mesomerie: unterschiedliche Darstellung des Benzolmoleküls. Valenzstrichformel (a), zwei mesomere Grenzstrukturen des Benzols (b, c) und alternative Darstellung als aromatisches System (d). Mesomerie: unterschiedliche Darstellung des Benzolmoleküls. Valenzstrichformel (a), zwei mesomere Grenzstrukturen des Benzols (b, c) und alternative Darstellung als aromatisches System (d). |
|