| |
chemische Reaktionen finden mit einer endlichen Geschwindigkeit statt, die von
wenigen Nanosekunden bis Jahrtausende betragen kann (Abb. 1). Überlegungen zur Kinetik einer
Reaktion sind daher unverzichtbare Ergänzung zu thermodynamischen Ansätzen, insbesondere in
offenen Systemen. Für eine schematisierte Reaktion: A+2B→3C kann die Reaktionsrate als Zunahme des Produktes C bzw. als Abnahme der Edukte A oder B über
die Zeit definiert werden:
Rate=d{C}/dt=-3d{A}/dt=-3/2·d{B}/dt, mit {}=chemische Aktivität der Substanzen. Die Ordnung der Reaktion bezeichnet dabei die
Abhängigkeit der Rate von der Aktivität der jeweiligen Substanz: Rate=k·{A}α·{B}β·{C}γ .
Die Ordnung der Gesamtreaktion ist dann die Summe der Potenzen α, β und γ. Die Ratenkonstante k (spezifische Rate) ist gleich der Reaktionsrate, wenn alle Reaktanden mit der Aktivität 1 vorliegen. Für eine einfache Reaktion A→B demonstriert Abb. 2 den Einfluss der Reaktionsordnung auf die Beziehungen von Aktivität und Zeit bzw. Aktivität und Reaktionsrate. Die Reaktionsrate ist stark abhängig von der Temperatur. Die Änderung der Reaktionskonstante k mit der Temperatur wird durch die Arrhenius-Gleichung beschrieben:
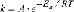 mit A=Konstante, Ea=Aktivierungsenergie, R=Gaskonstante, T=Temperatur. mit A=Konstante, Ea=Aktivierungsenergie, R=Gaskonstante, T=Temperatur.
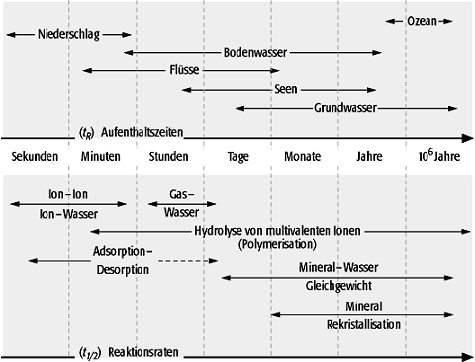 Reaktionsrate 1: Vergleich der Raten verschiedener chemischer Reaktionen (ausgedrückt als Halbwertszeiten t1/2) und der Aufenthaltszeit von Wasser in verschiedenen Reservoiren der Hydrosphäre. Reaktionsrate 1: Vergleich der Raten verschiedener chemischer Reaktionen (ausgedrückt als Halbwertszeiten t1/2) und der Aufenthaltszeit von Wasser in verschiedenen Reservoiren der Hydrosphäre.
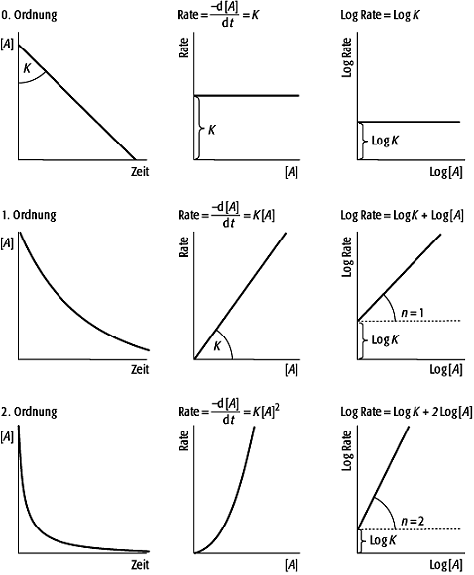 Reaktionsrate 2: Einfluss der Reaktionsordnung auf die Aktivitätsänderung mit der Zeit und die Beziehung der Reaktionsrate zur Aktivität des Ions A für die schematische Reaktion A→B. Reaktionsrate 2: Einfluss der Reaktionsordnung auf die Aktivitätsänderung mit der Zeit und die Beziehung der Reaktionsrate zur Aktivität des Ions A für die schematische Reaktion A→B. |
|